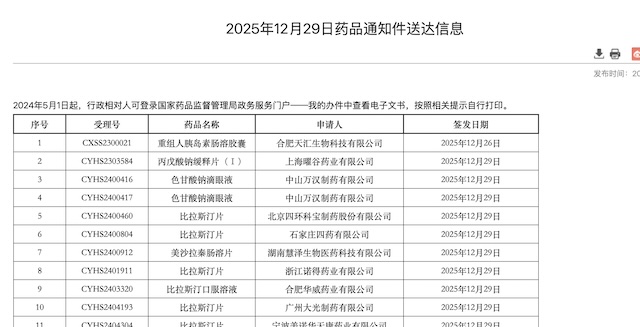
12月29日,國家藥監局網站公布的藥品通知件送達信息顯示,合肥天匯生物科技有限公司(下稱天匯生物)申請的重組人胰島素腸溶膠囊位于其中。
一般而言,拿到藥品通知件,有可能是藥品上市申請“不予批準”,或者是企業因預判無法過審而主動撤回上市申請。
第一財經記者亦向天匯生物方面了解這款藥上市申請未能成功原因,截至發稿之際,還未獲得回復。
之所以重組人胰島素腸溶膠囊備受關注,原因在于它是全球范圍第一個申報上市的口服胰島素,最早于2023年4月在中國申報上市,用于治療口服降糖藥療效不佳的2型糖尿病患者。
天匯生物的這款重組人胰島素腸溶膠囊,也是一款引進產品,來自于以色列Oramed公司。
長久以來,在糖尿病的藥物治療中,胰島素一直占據著不可替代的地位,盡早起始胰島素治療對糖尿病患者的病情管理起到至關重要的作用,但由于皮下注射給藥方式的局限性,部分患者對于胰島素的使用依舊心存顧慮,導致起始胰島素治療時機延后,影響患者的血糖達標。如何改善胰島素用藥方式、實現胰島素口服給藥,是百年來科學家們試圖攻克的難題。
然而,口服胰島素的開發并不容易,海外的胰島素巨頭們也遭遇過開發失敗。胰島素是由多個氨基酸合成的肽類物質,屬于蛋白質類激素,分子量大、易被酶降解、滲透性低,經口服吸收進入靶器官發揮生理作用之前,需要闖過化學、酶、滲透三道屏障,即胃腸道內復雜多變的酸堿環境,消化系統包含的多種蛋白酶,以及在滲透環節中因腸道上皮細胞緊密排列產生的狹窄通道、與杯狀細胞形成的黏膜屏障。
事實上,天匯生物的這款口服胰島素產品在國內申請上市時,也曾引發過爭議,原因是在國外的三期臨床試驗已經失敗了。2023年1月,Oramed公司曾宣布,口服胰島素膠囊ORMD-0801(重組人胰島素腸溶膠囊)即治療2型糖尿病的三期臨床試驗(ORA-D-013-1研究)未達到主要終點和次要終點。
此次重組人胰島素腸溶膠囊上市申請未能成功,會對天匯生物后續的投入帶來怎樣影響,有待后續關注。
幫企客致力于為您提供最新最全的財經資訊,想了解更多行業動態,歡迎關注本站。鄭重聲明:本文版權歸原作者所有,轉載文章僅為傳播更多信息之目的,如作者信息標記有誤,請第一時間聯系我們修改或刪除,多謝。



